Continua após publicidade
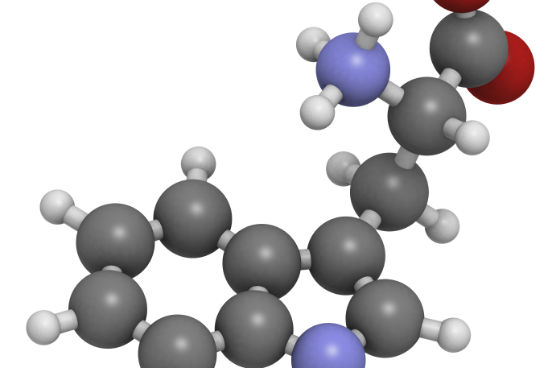
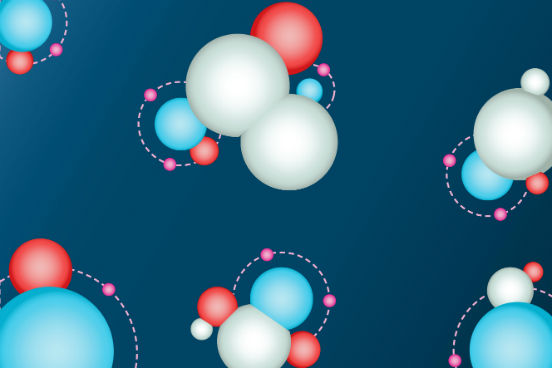
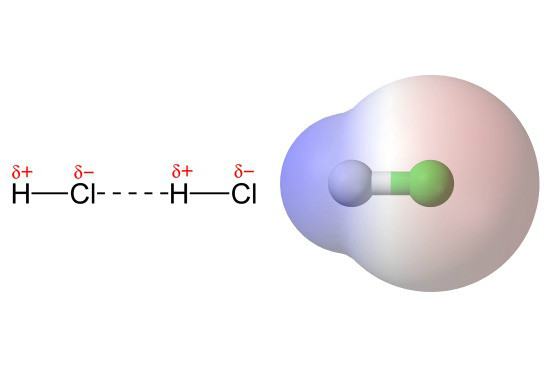
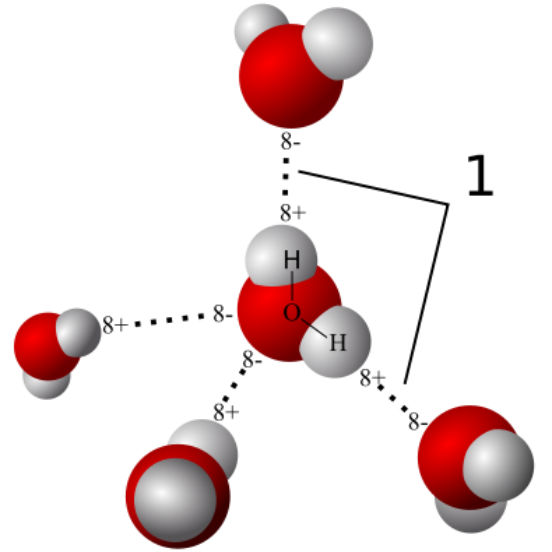
Forças intermoleculares
Além de manterem próximas as moléculas de uma substância, as forças intermoleculares influenciam em propriedades como ponto de fusão e ebulição. Saiba mais
















Essa é uma matéria exclusiva para assinantes. Se você já é assinante faça seu login
Este usuário não possui direito de acesso neste conteúdo. Para mudar de conta, faça seu login

Não vá embora sem ler essa matéria!
Assista um anúncio e leia grátis
CLIQUE AQUI.